Đây là sự kiện quan trọng trong ung thư phổi và cũng là sự kiện quan trọng trong điều trị miễn dịch.
Phê chuẩn này dựa trên nghiên cứu pha III KEYNOTE-024 gồm 2 nhánh:
- pembrolizumab (Keytruda) , 200mg IV (n = 154)
- Hóa trị: pemetrexed/carboplatin hoặc Gem/platin hoặc Docetacel (n = 151)
Các bn này phải có PD-L1 + hơn 50%, EGFR-, ALK -
Kết quả:
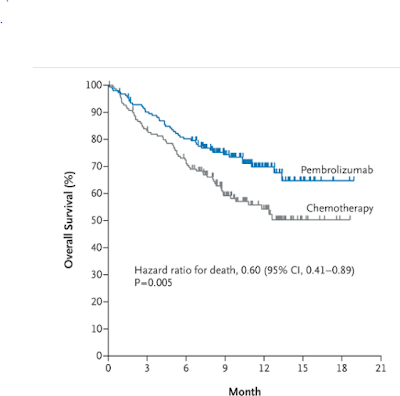
- 6-month overall survival (OS)
80.2% pembrolizumab sv
72.4% cho hoá trị (HR, 0.60; 95% CI, 0.41-0.89; P = .005).
- PFS
10.3 tháng pembrolizumab sv
6.0 tháng cho hoá trị (HR, 0.50; 95% CI, 0.37-0.68; P <.001).
- 6-month PFS:
62.1% pembrolizumab sv
50.3% hoá trị.
- Objective response rate:
pembrolizumab 44.8%
hoá trị 27.8%
2. Nghiên cứu Keynote đã được trình bày lần đầu tại ESMO 2016 tháng 10/2016 bởi M. Reck, Department of Thoracic Oncology, Hospital Grosshansdorf, Wohrendamm 80, 22927 Grosshansdorf, Germany thật sự là một nghiên cứu changing practice !
3. Một cuộc động đất ?
Tờ Medscape đưa tin như vậy, có quá đáng hay không ?
Theo họ phân tích:
- Hoá trị cho đến nay vẫn được xem là big gorilla. Rất khó hạ gục
- EGFR TKIs chỉ có giá trị với 15% trường hợp UTPKTBN (có EGFR+), 5% là có ALL hoặc ROS1+,có thể dùng crizotinib, 80% trường hợp còn lại phải nhường bước cho hoá trị.
Nay pembrolizumab chỉ cần đòi hỏi PD-L1+ 50% là đủ, chiếm gần 40% các trường hợp UTPKTBN
4. Cuộc chạy đua
Các thuốc điều trị miễn dịch mà nói đúng hơn là các thuốc ức chế điểm gác miễn dịch đã có một cuộc đua từ 4 năm qua.
Chặng đầu tiên: chinh phục bước 2.
Nivolumab đã về đích trước với 2 nghiên cứu Checkmate 017 và Checkmate 057;
Pembrolizumab về nhì với nghiên cứu Keynote 010
Trang này đã đề cập đến qua nhiều bài
Atezolizumab về đích thứ 3 qua nghiên cứ OAK
Pembrolizumab (Keytruda) được FDA phê chuẩn hoàn toàn trong ung thư phổihttp://nguyentuankhoi.blogspot.com/2016/03/pembrolizumab-keytruda-uoc-fda-phe.html
Chặng cuối: chinh phục bước 1
Pembrolizumab đã về đích đầu tiên





No comments:
Post a Comment